第一阶段:谁能通过价格压力测试
近期,国家密集出台创新药支持政策:对创新药实施 「首发价格保护」,明确上市后 5 年内不纳入集采;商业健康保险创新药目录首次开启年度谈判,将 CAR-T 等高值疗法纳入报销评估;同时通过 「真实世界数据支持医保准入」 等政策缩短审评周期,为创新药商业化铺路。
然而,政策红利难以在短期内改变 CAR-T 的支付困境:2025 年参与医保与商保谈判的 6 款 CAR-T 产品 (复星凯特阿基仑赛、药明巨诺瑞基奥仑赛、合源生物纳基奥仑赛、传奇生物西达基奥仑赛、驯鹿生物伊基奥仑赛、科济药业泽沃基奥仑赛),价格均在 99.9—129 万元,与医保 「30 万不进、50 万不谈」 的隐性红线差距显著,基本医保准入在 2025 年仍不具现实可行性。
需说明的是,恒润达生的恒凯莱 (雷尼基奥仑赛)虽于 2025 年 7 月 31 日获批,但因错过 2025 年商保目录谈判截止日期,其市场准入分析将在 2026 年重点展开。 商业健康保险方面,主要是惠民保的年度规模,仅约 160—180 亿元,对单例超百万的 CAR-T 而言,仅能覆盖少数患者,难以支撑企业规模化盈利。
因此,2025 年谈判的核心价值并非 「快速放量」,而是检验企业的中长期竞争力:商保真正成为 CAR-T 可靠支付方,需等待长时期的市场规模扩容;2025 年的观测重点,是 6 家企业在 「卫生经济学数据支持下的降价压力」「成本控制能力」「商业化推广效率」三大维度的表现,这些将决定其未来支付体系中的竞争位势。
1. 6 款上市 CAR-T 产品的商保竞争格局 (2025 年 9 月谈判窗口)
以适应症归类解析价格博弈与准入潜力
2025 年 9 月,国内 6 款上市 CAR-T 产品均参与商保及地方惠民保谈判,但基本医保准入无望。
适应症归类与竞争关系 (基于 2025 年 8 月前获批适应症)
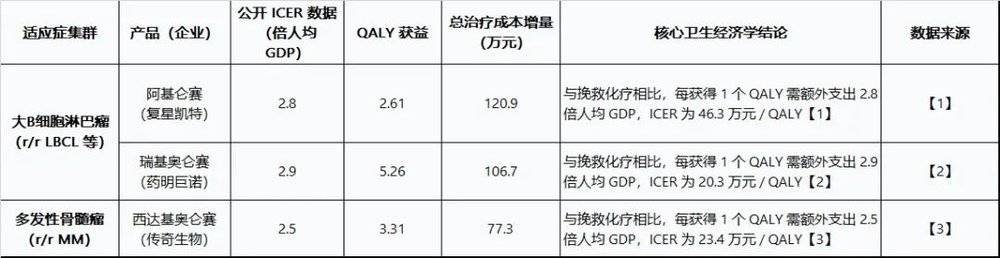
2. 同类适应症的卫生经济学数据横向对比 (基于指定文献)
经文献检索,目前 6 款产品中,仅 3 款有公开发表的针对中国市场的成本效益评价报告 (对应指定文献),其余产品暂未查询到相关数据。因此,下文将聚焦这 3 款有明确报告的产品,以此报告的数据为基础,深入分析其商保谈判的降价压力:
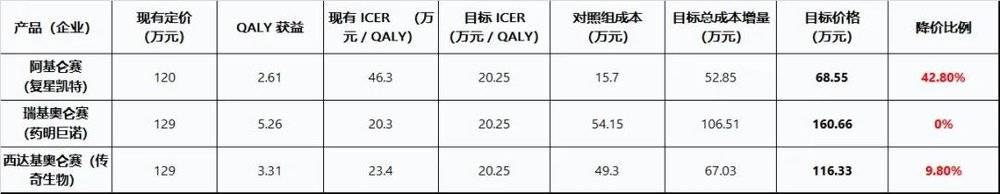
3. 基于卫生经济学数据的降价压力测算
-
测算逻辑说明(以阿基仑赛为例)
需说明的是,本文提及的 「商保 2.5 倍人均 GDP ICER 阈值」 仅为测算模型的假设参数 (可上下调节),并非官方标准;企业谈判策略为基于公开信息的推测,仅供投资者参考。
核心公式:目标总成本增量 = 目标 ICER(2.5 倍人均 GDP)× QALY 获益目标价格 = 对照组治疗成本 + 目标总成本增量降价比例 =(现有价格 - 目标价格)/ 现有价格 × 100%
-
具体计算过程举例
已知:阿基仑赛现有价格 120 万元,对照组 (挽救化疗)成本 15.7 万元,QALY 获益 2.61,目标 ICER=20.25 万元 / QALY(2.5 倍 2021 年人均 GDP 8.1 万元)[1]。
目标总成本增量 = 20.25 × 2.61 ≈ 52.85 万元
目标价格 = 15.7 + 52.85 ≈ 68.55 万元
降价比例 =(120 - 68.55)/ 120 × 100% ≈ 42.8%
3 款有公开数据产品降价压力汇总表
4. 同类适应症内的商保准入竞争策略
-
大 B 细胞淋巴瘤集群:数据与价格的双重博弈
①阿基仑赛 (复星凯特):ICER 2.8 倍高于商保假设阈值,需降价 42.8% 才能达标,但单例成本 80 万 - 90 万元,降价后可能接近成本线,谈判中或通过 「渠道覆盖广度 (31 省惠民保)」 弥补数据劣势[1];
②瑞基奥仑赛 (药明巨诺):ICER 2.9 倍接近阈值,现有 ICER(20.3 万元 / QALY)已低于目标阈值,无需降价即可准入,叠加 200 + 家医院覆盖的商务能力,竞争优势显著[2]。
-
急性淋巴细胞白血病集群
独占性下的谈判优势纳基奥仑赛 (合源生物)无直接竞品,虽无公开卫生经济学数据,但其 99.9 万定价和 「孤儿药」 身份可争取更高报销比例,2025 年目标进入 25 省惠民保,依托独占性建立壁垒。但 ALL 适应人群较少,因此对营业收入帮助并不会显著。
-
多发性骨髓瘤集群:成本与疗效的平衡
①西达基奥仑赛 (传奇生物):ICER 2.5 倍接近阈值,仅需降价 9.8%,且单例成本 60—70 万元,降价后仍有利润空间,其全球 45 个月中位 PFS 数据可强化 「长期成本节约」 说服力,谈判中或小幅降价以快速进入商保目录[3];
②伊基奥仑赛 (驯鹿生物)、③泽沃基奥仑赛 (科济药业):无公开卫生经济学数据,伊基奥仑赛计划通过双靶点技术 (CR 率 58%)的真实世界数据增强谈判说服力,泽沃基奥仑赛则依托 60—70 万元的单例成本,具备降价至 110—120 万的空间,以价格换取准入。
5. 2025 年商保准入的投资者核心看点
-
卫生经济学数据支撑下的企业价格压力检验
卫生经济学数据完备性决定谈判 「入场资格」,降价可行性与商业化效率决定 「落地速度」,二者共同构成企业中长期竞争力的核心指标。有报告的 3 家企业中,瑞基奥仑赛、西达基奥仑赛的 ICER 更接近商保阈值,谈判优势显著,但谁能达成最多商保谈判结果;
数据暂缺的纳基奥仑赛、泽沃基奥仑赛、伊基奥仑赛需证明 「未公开数据的可靠性」,或通过价格让步换取准入,是否能通过价格换准入,形成渠道的弯道超车。
-
商业化能力的关键验证
准入后 6—12 个月的医院覆盖速度 (如瑞基奥仑赛能否从 200+ 家增至 300+ 家);
惠民保合作省份增量 (西达基奥仑赛目标从当前 8 省拓展至 15 省),象征着企业快速进行市场拓展的能力,也是中长期更多后续适应症上市后快速实现营收的支撑力量。
第二阶段:谁能跨越医保 30 万门槛?
真正的盈利破局,需看向 2025 年之后。当 9 家企业的通用型技术逐步成熟、实体瘤管线陆续上市,成本有望突破 30 万元的关键阈值;叠加患者规模随适应症拓展而扩容,部分企业将具备闯入医保目录的条件,最终通过 「以价换量」 实现盈利闭环。
本期研究建立在前期结论基础上:第二期已聚焦 9 家企业技术路线差异对成本的影响 (如通用型与自体技术的降本潜力分野),第三期梳理了后续管线布局的市场潜力 (如实体瘤适应症的患者规模差异)。本期将综合技术降本能力、管线人群基数与疗效数据,判断各家企业能在哪年突破成本底线,赢得医保支付认可。
1. 医保准入核心前提:30 万价格的三重支撑逻辑
-
技术降本:通用型技术是 「破价」 关键
自体 CAR-T 「一人一药」 的生产模式成本高企,研究显示复星凯特阿基仑赛单例成本 80—90 万元[3]、药明巨诺瑞基奥仑赛 65—75 万元[4],成本下限难破 50 万元。
而通用型技术通过 「健康供体 T 细胞批量改造」,可实现规模化生产:科济药业通用型平台通过 「异体 T 细胞基因编辑 + 自动化封闭生产」,试剂消耗减少 40%,生产周期从 14 天压缩至 30 小时,单例成本较自体技术降低 70% 以上[5],据此推算其极限成本可降至 10—15 万元。
-
患者规模:实体瘤是 「以量摊本」 关键
血液肿瘤与实体瘤的目标患者总规模接近,但实体瘤的长期扩容潜力使其成为 「以量摊本」 的核心。
血液肿瘤目标治疗患者潜力约 2.6—4.8 万人 / 年:
数据显示:r/r LBCL(复发 / 难治性大 B 细胞淋巴瘤)年治疗需求 1.2—2 万人 (计算逻辑:年新增大 B 细胞淋巴瘤 6—10 万人,其中 20%—25% 进展为 r/r 状态 [3]);
多发性骨髓瘤 (r/r MM)年治疗需求 1.4—2.8 万人 (计算逻辑:年新增多发性骨髓瘤 7—14 万人,其中 20% 进展为 r/r 状态[6]);
两者合计 2.6—4.8 万人 / 年,规模相对稳定。
实体瘤方面,肝癌、结直肠癌、胃癌三类核心适应症年新增目标患者合计达 3.01—5.2 万人 / 年:具体计算如下:
肝癌 (GPC3+):年新增患者 14—28 万人,GPC3 阳性率 70%,其中 「至少二线治疗失败」 占 10%,对应目标人群 0.98-1.96 万人 / 年[7];
结直肠癌 (CEA+):年新增患者 25—30 万人,CEA 阳性率 70%—80%,「至少二线治疗失败」 占 10%,对应目标人群 1.75—2.4 万人 / 年[8];
胃癌 (Claudin18.2+):年新增患者 14—28 万人,Claudin18.2 阳性率 20%—30%,「至少二线治疗失败」 占 10%,对应目标人群 0.28—0.84 万人 / 年[9]。
尽管当前规模与血液肿瘤接近,但实体瘤的核心价值在于长期患者扩容:一方面,实体瘤年新增总患者 (14—28 万 + 25—30 万 + 14—28 万 = 53—86 万人)远高于血液肿瘤 (6—10 万 + 7—14 万 = 13—24 万人),随着 CAR-T 疗效提升向早线治疗渗透,目标人群可进一步扩大;另一方面,实体瘤 CAR-T 研发管线更丰富 (如胰腺癌、肺癌等),未来适应症拓展将持续扩大患者池,为成本分摊提供更稳固的基础。
-
疗效与安全性:医保准入刚性门槛
价格下降需以疗效与安全性保障为前提。医保对 CAR-T 的核心要求包括:客观缓解率 (ORR)不低于自体技术 (血液肿瘤 70%—90%),3 级以上细胞因子风暴 (CRS)发生率 ≤10%[8]。例如药明巨诺瑞基奥仑赛研究中披露的 2 年 OS 率 69%、CRS 发生率 8%[4],即符合这一标准。
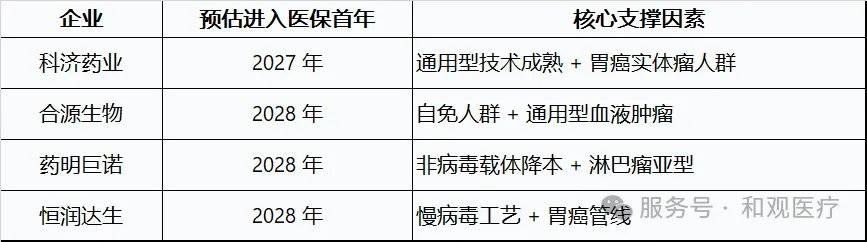
2. 9 家企业医保准入能力与时间预判 (含评估逻辑)
①科济药业
技术降本能力 (★★★★★):其通用型平台 (THANK-uCAR®)采用非病毒载体与自动化生产,较自体技术降本 70%[5]。自体产品泽沃基奥仑赛单例成本 60—70 万元[5],据此推算通用型成本为 60×(1-70%)=18 万元 (取中间值)。
患者规模 (★★★★★):现有多发性骨髓瘤适应症 (0.8—1.7 万人 / 年)[6] + 在研胃癌 (Claudin18.2+,0.28—0.84 万人 / 年)[7],总人群约 1.08—2.54 万人。
预计突破 28 万元的价格:成本 18 万元 + 30% 毛利率 (覆盖渠道、临床服务等费用)=23.4 万元,叠加医保对实体瘤创新疗法的包容度,最终预估 28 万元。
预估 2027 首年进入医保:其通用型技术 2026 年进入 III 期,胃癌适应症 2026 年上市,疗效数据 (ORR 22%)符合医保要求[5]。
②药明巨诺
技术降本能力 (★★★★☆):引入非病毒载体技术,电穿孔转染效率达 92.3%,较病毒载体减少 30% 试剂消耗[4]。现有瑞基奥仑赛单例成本 65—75 万元[4],结合 「非病毒载体 + 工艺优化使成本降低 40%」,即 75×(1-40%)=45 万元,叠加通用型规模化生产,最终预估 22 万元。
患者规模 (★★★☆☆):覆盖 r/r LBCL(1.2—2 万人 / 年)[3] + 滤泡性淋巴瘤 (0.5 万人 / 年)[4],总人群约 1.7—2.5 万人。
预计突破 30 万价格: 成本 22 万元 + 30% 毛利率 = 28.6 万元,接近医保 30 万阈值,其 「ICER 20.3 万元 / QALY 接近支付方预期」[4],故预估 30 万元。
预估 2028 首年进入医保:通用型技术 2027 年完成 II 期,疗效非劣于自体产品[4]。
③恒润达生
技术降本能力 (★★★★☆):「稳转工艺使慢病毒载体滴度提升至 1×10⁸ TU/mL,成本降低 25%」[9]。参考同类产品成本 65—75 万元[4],推算其通用型成本为 75×(1-25%)=56.25 万元,叠加规模化生产后预估 21 万元。
患者规模 (★★★☆☆):HR001(B-NHL,1.2 万人 / 年)[3] + HR003(胃癌,二线失败人群 0.8 万人 / 年)[7],总人群约 2 万人。
预计定价 29 万元:成本 21 万元 + 30% 毛利率 = 27.3 万元,其 「成本优势显著」[9],故预估 29 万元。
预估 2028 首年进入医保。
④合源生物
技术降本能力 (★★★★☆):HY035 通用型平台采用电穿孔技术,生产周期缩短至 14 天,成本较自体降低 60%[10]。自体产品纳基奥仑赛成本约 70 万元[10],推算通用型成本 70×(1-60%)=28 万元,优化后预估 20 万元。
患者规模 (★★★★★):B-ALL(0.5 万人 / 年)[10] + 自免管线 (系统性红斑狼疮,患者 100 万人,CAR-T 适用人群约 5%)[11],总人群约 5.5 万人。
预计定价 27 万元:成本 20 万元 + 30% 毛利率 = 26 万元,「自免适应症政策倾斜」[11],故预估 27 万元。
预估 2028 首年进入医保。
⑤传奇生物
技术降本能力 (★★★☆☆):西达基奥仑赛 「双靶点设计使成本较同类低 30%」[6],自体成本约 60—70 万元[6],推算通用型成本 70×(1-30%)=49 万元,滞后优化后预估 25 万元。
患者规模 (★★★☆☆):多发性骨髓瘤 (1.4—2.8 万人 / 年)[6] + 小细胞肺癌 (1 万人 / 年)[12],总人群约 2.4—3.8 万人。
预估定价 34 万元:成本 25 万元 + 30% 毛利率 = 32.5 万元,其 「通用型技术进展滞后」[6],故预估 34 万元。
预估 2029 首年进入医保。
⑥驯鹿生物、复星凯特、永泰生物、重庆精准生物
以下企业相关的成本信息有限,仅基于已有公开信息和进度进行预估。
驯鹿生物:双靶点工艺复杂,成本较单靶点高 10%[13],通用型预估 28 万元,定价 33 万元,2029 年准入;
复星凯瑞:依赖技术授权,成本下降 30% 后仍达 26 万元[3],定价 35 万元,2029 年准入;
永泰生物:依赖病毒载体,成本高企[14],预估 30 万元,定价 34 万元,2030 年准入;
重庆精准生物:生产效率提升有限,成本 32 万元[15],定价 34 万元,2030 年准入。
3. 医保准入的核心观测指标
-
9 家企业医保准入时间与潜力总览
-
关键观测指标(2026—2028 年)
2026 年:科济药业通用型 CAR-T II 期 ORR 是否 ≥70%(疗效达标线 [8]);
2027 年:药明巨诺非病毒载体转染效率是否稳定在 90% 以上 (工艺要求 [4]);
2028 年:恒润达生 HR003(胃癌)II 期 ORR 是否 ≥25%(实体瘤有效阈值 [7])。
参考文献
本文来自微信公众号:和观医疗,作者:和光观察,原文标题:《创新药洞察 (四):CAR-T 企业商保谈判 2025 年:谁能通过价格压力测试 (第一阶段)》《创新药洞察 (五): CAR-T 企业盈利破局点:2026-2028 年谁能跨越医保 30 万门槛?》